Energi ionisasi dan afinitas elektron.
Jika kamu mencari artikel energi ionisasi dan afinitas elektron terbaru, berarti kamu telah berada di blog yang benar. Yuk langsung saja kita simak penjelasan energi ionisasi dan afinitas elektron berikut ini.
 Jelaskan Hubungan Antara Descubre Como Resolverlo En Qanda From qanda.ai
Jelaskan Hubungan Antara Descubre Como Resolverlo En Qanda From qanda.ai
O g e O g Electron Affinity. Karena energi dilepas maka harga afinitas elektron diberi tanda minus. Semakin besar energi yang dilepas ion negatif yang terbentuk semakin stabil. Harga afinitas elektronnya positifDalam satu periode dari kiri ke kanan nilai afinitas elektron cenderung meningkat.
Dengan demikian energi ionisasi n 1 selalu lebih tinggi daripada n th energi ionisasi.
Energi Ionisasi vs Afinitas Elektron. Energi ionisasi adalah jumlah energi yang dibutuhkan untuk melepaskan elektron dari atom netral. Harga voltase pada saat mulai terjadinya arus listrik inilah yang didefinisikan sebagai energi ionisasi. Unsur golongan IIA dan VIIIA tidak membentuk ion negatif yang stabil. Atom adalah blok bangunan kecil dari semua zat yang ada.
 Source: nawikimia.com
Source: nawikimia.com
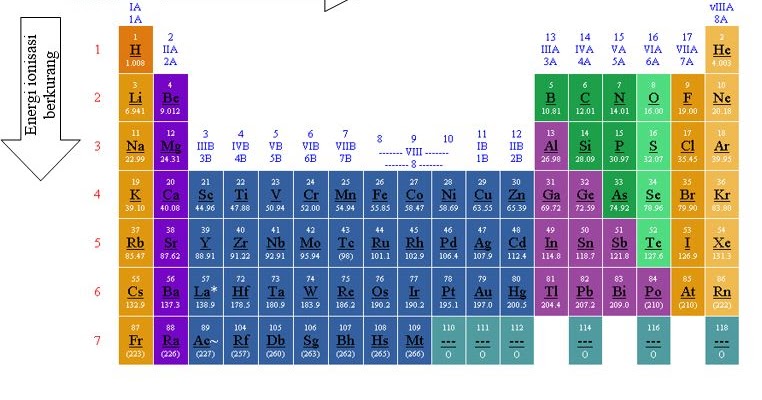
Semakin besar daya tarik electron semakin besar energi ionisasi juga semakin besar semakin negatif afinitas elektron. Potensial Ionisasi atau energi ionisasi adalah energi minimum yang diperlukan oleh suatu atom netral atau ion untuk melepas 1 buah elektron yang terikat paling luar dalam fase gas. Definisi ini dapat digunakan pada n 0. Sifat Keperiodikan Energi Ionisasi Energi ionisasi adalah energi yang diperlukan suatu atom untuk melepaskan satu elektron valensi membentuk ion positif. Akibatnya jari-jari atom makin kecil energi ionisasi makin besar afinitas elektron makin besar makin negatif dan kecenderungan untuk menarik elektron makin besar.
Semakin besar energi yang dilepas ion negatif yang terbentuk semakin stabil.
Selain neutron dan positron ada partikel sub atom kecil lainnya di. Karena energi dilepas maka harga afinitas elektron diberi tanda minus. Potensial Ionisasi atau energi ionisasi adalah energi minimum yang diperlukan oleh suatu atom netral atau ion untuk melepas 1 buah elektron yang terikat paling luar dalam fase gas. Energi ionisasi dan afinitas elektron berkaitan dengan besarnya daya tarik elektron.
 Source: qanda.ai
Source: qanda.ai
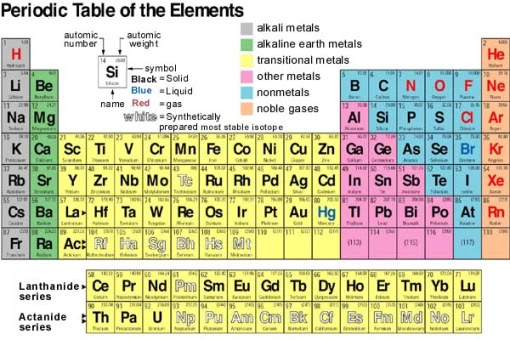
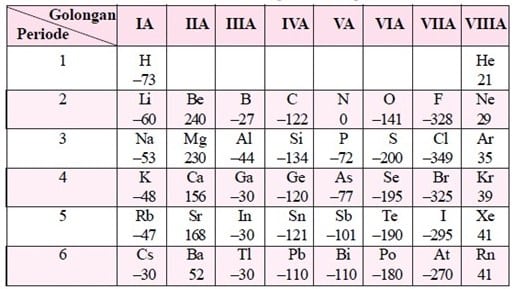
Secara konvensional definisi energi afinitas adalah energi yang dibebaskan bila tiap mol atom netral atau ion dalam keadaaan gas menangkap elektron membentuk ion negatif. - Melepaskan Energi Karena. Oleh karena itu energi ionisasi biasanya dinyatakan dalam satuan SI elektron volt eV 1 eV 160 10 19 J 96485 kJmol 1 dan sering pula disebut sebagai potensial ionisasi. Membutuhkan Energi -.
 Source: kimia100.com
Source: kimia100.com
Oleh karena itu energi ionisasi biasanya dinyatakan dalam satuan SI elektron volt eV 1 eV 160 10 19 J 96485 kJmol 1 dan sering pula disebut sebagai potensial ionisasi. Perhatikanlah Gambar 110 dalam satu golongan dari atas ke bawah jumlah kulit bertambah sehingga jarak elektron valensi ke inti atom bertambah dan elektron lebih mudah lepas. Potensial Ionisasi atau energi ionisasi adalah energi minimum yang diperlukan oleh suatu atom netral atau ion untuk melepas 1 buah elektron yang terikat paling luar dalam fase gas. Ketika elektron terletak lebih dekat ke inti energi ionisasi meningkat.
 Source: rumusrumus.com
Source: rumusrumus.com
Karena energi dilepas maka harga afinitas elektron diberi tanda minus. Semakin besar energi yang dilepas ion negatif yang terbentuk semakin stabil. Potensial Ionisasi atau energi ionisasi adalah energi minimum yang diperlukan oleh suatu atom netral atau ion untuk melepas 1 buah elektron yang terikat paling luar dalam fase gas. Akibatnya jari-jari atom makin kecil energi ionisasi makin besar afinitas elektron makin besar makin negatif dan kecenderungan untuk menarik elektron makin besar.
Unsur golongan IIA dan VIIIA tidak membentuk ion negatif yang stabil. Karena energi dilepas maka harga afinitas elektron diberi tanda minus. Sifat Keperiodikan Energi Ionisasi Energi ionisasi adalah energi yang diperlukan suatu atom untuk melepaskan satu elektron valensi membentuk ion positif. Selain itu ketika membandingkan dua energi ionisasi.
Energi ionisasi berhubungan dengan pembuatan kation dari atom netral dan afinitas elektron berhubungan dengan.
Afinitas Elektron adalah Energi baik yang dibutuhkan maupun yang dilepaskan oleh atomion berfase gas untuk menangkap 1 elektron ket. Semakin besar daya tarik electron semakin besar energi ionisasi juga semakin besar semakin negatif afinitas elektron. Afinitas elektron adalah ukuran energi yang dilepaskan ketika atom netral dalam fasa gas memperoleh elektron dan membentuk ion bermuatan negatif anion. Energi ionisasi Energi ionisasi adalah energi yang diperlukan untuk melepaskan elektron yang terikat paling lemah. Harga voltase pada saat mulai terjadinya arus listrik inilah yang didefinisikan sebagai energi ionisasi.
 Source: sites.google.com
Source: sites.google.com
Energi ionisasi dan afinitas elektron berkaitan dengan besarnya daya tarik elektron. Afinitas elektron adalah ukuran energi yang dilepaskan ketika atom netral dalam fasa gas memperoleh elektron dan membentuk ion bermuatan negatif anion. Energi ionisasi adalah jumlah energi yang dibutuhkan untuk melepaskan elektron dari atom netral. Harga voltase pada saat mulai terjadinya arus listrik inilah yang didefinisikan sebagai energi ionisasi. Semakin besar energi yang dilepas ion negatif yang terbentuk semakin stabil.
O g e O g Electron Affinity. Afinitas elektron adalah ukuran energi yang dilepaskan ketika atom netral dalam fasa gas memperoleh elektron dan membentuk ion bermuatan negatif anion. Dengan demikian energi ionisasi n 1 selalu lebih tinggi daripada n th energi ionisasi. Semakin besar daya tarik electron semakin besar energi ionisasi juga semakin besar semakin negatif afinitas elektron.
Harga voltase pada saat mulai terjadinya arus listrik inilah yang didefinisikan sebagai energi ionisasi.
Dengan demikian proses yang terjadi dapat dipandang sebagai kebalikan dari proses pelepasan elektron yaitu. Jari-jari atom O Kecil Mudah Menarik elektron Tarikan Inti besar Tolakan antar elektron kecil O e - O 2-Electron Affinity. Membutuhkan Energi -. 261 Energi ionisasi dan afinitas elektron Energi yang diperlukan untuk membuat n1 keadaan valensi ionik dengan mengeluarkan sebuah elektron dari keadaan valensi ionik n dari sebuah bahan disebut sebgai energi ionisasi ke n1.
 Source: slideplayer.info
Source: slideplayer.info
Dengan demikian energi ionisasi n 1 selalu lebih tinggi daripada n th energi ionisasi. Ketika elektron terletak lebih dekat ke inti energi ionisasi meningkat. Semakin besar energi yang dilepas ion negatif yang terbentuk semakin stabil. Energi ionisasi berhubungan dengan pembuatan kation dari atom netral dan afinitas elektron berhubungan dengan.
 Source: brainly.co.id
Source: brainly.co.id
261 Energi ionisasi dan afinitas elektron Energi yang diperlukan untuk membuat n1 keadaan valensi ionik dengan mengeluarkan sebuah elektron dari keadaan valensi ionik n dari sebuah bahan disebut sebgai energi ionisasi ke n1. Ketika elektron terletak lebih dekat ke inti energi ionisasi meningkat. O g e O g Electron Affinity. Energi Ionisasi vs Afinitas Elektron.
 Source: kimia-science7.com
Source: kimia-science7.com
Atom adalah blok bangunan kecil dari semua zat yang ada. Dengan demikian energi ionisasi n 1 selalu lebih tinggi daripada n th energi ionisasi. Atom adalah blok bangunan kecil dari semua zat yang ada. Sifat Keperiodikan Energi Ionisasi Energi ionisasi adalah energi yang diperlukan suatu atom untuk melepaskan satu elektron valensi membentuk ion positif.
Jari-jari atom O Kecil Mudah Menarik elektron Tarikan Inti besar Tolakan antar elektron kecil O e - O 2-Electron Affinity.
Semakin besar energi yang dilepas ion negatif yang terbentuk semakin stabil. 261 Energi ionisasi dan afinitas elektron Energi yang diperlukan untuk membuat n1 keadaan valensi ionik dengan mengeluarkan sebuah elektron dari keadaan valensi ionik n dari sebuah bahan disebut sebgai energi ionisasi ke n1. Harga voltase pada saat mulai terjadinya arus listrik inilah yang didefinisikan sebagai energi ionisasi. Semakin besar daya tarik electron semakin besar energi ionisasi juga semakin besar semakin negatif afinitas elektron. Semakin besar energi yang dilepas ion negatif yang terbentuk semakin stabil.
 Source: slidetodoc.com
Source: slidetodoc.com
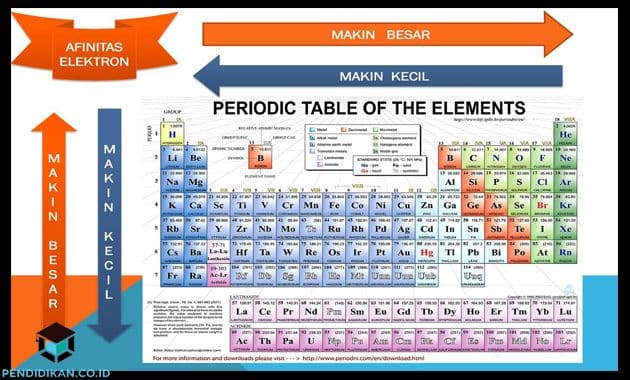
Afinitas elektron adalah ukuran energi yang dilepaskan ketika atom netral dalam fasa gas memperoleh elektron dan membentuk ion bermuatan negatif anion. Akibatnya jari-jari atom makin kecil energi ionisasi makin besar afinitas elektron makin besar makin negatif dan kecenderungan untuk menarik elektron makin besar. - Melepaskan Energi Karena. Membutuhkan Energi -. Harga afinitas elektronnya positifDalam satu periode dari kiri ke kanan nilai afinitas elektron cenderung meningkat.
Jari-jari atom O Kecil Mudah Menarik elektron Tarikan Inti besar Tolakan antar elektron kecil O e - O 2-Electron Affinity.
Karena energi dilepas maka harga afinitas elektron diberi tanda minus. Dengan demikian energi ionisasi n 1 selalu lebih tinggi daripada n th energi ionisasi. Energi Ionisasi versus Afinitas Elektron Tren lain yang terlihat pada tabel periodik adalah afinitas elektron. Ini meningkatkan energi ionisasi atom kecil.
 Source: qanda.ai
Source: qanda.ai
Ini meningkatkan energi ionisasi atom kecil. Definisi ini dapat digunakan pada n 0. Potensial Ionisasi atau energi ionisasi adalah energi minimum yang diperlukan oleh suatu atom netral atau ion untuk melepas 1 buah elektron yang terikat paling luar dalam fase gas. Unsur golongan IIA dan VIIIA tidak membentuk ion negatif yang stabil.

Selain neutron dan positron ada partikel sub atom kecil lainnya di. Oleh karena itu energi ionisasi biasanya dinyatakan dalam satuan SI elektron volt eV 1 eV 160 10 19 J 96485 kJmol 1 dan sering pula disebut sebagai potensial ionisasi. Ketika elektron terletak lebih dekat ke inti energi ionisasi meningkat. Atom adalah blok bangunan kecil dari semua zat yang ada.
 Source: pendidikan.co.id
Source: pendidikan.co.id
Cari tahu tentang energi ionisasi dan afinitas elektron yuk. Atom terdiri dari inti yang memiliki proton dan neutron. Energi Ionisasi versus Afinitas Elektron Tren lain yang terlihat pada tabel periodik adalah afinitas elektron. Afinitas elektron adalah ukuran energi yang dilepaskan ketika atom netral dalam fasa gas memperoleh elektron dan membentuk ion bermuatan negatif anion.
Energi Ionisasi versus Afinitas Elektron Tren lain yang terlihat pada tabel periodik adalah afinitas elektron.
261 Energi ionisasi dan afinitas elektron Energi yang diperlukan untuk membuat n1 keadaan valensi ionik dengan mengeluarkan sebuah elektron dari keadaan valensi ionik n dari sebuah bahan disebut sebgai energi ionisasi ke n1. Selain neutron dan positron ada partikel sub atom kecil lainnya di. Karena energi dilepas maka harga afinitas elektron diberi tanda minus. Atom terdiri dari inti yang memiliki proton dan neutron. Selain itu ketika membandingkan dua energi ionisasi.
 Source: rumusrumus.com
Source: rumusrumus.com
Jari-jari atom O Kecil Mudah Menarik elektron Tarikan Inti besar Tolakan antar elektron kecil O e - O 2-Electron Affinity. Semakin besar daya tarik electron semakin besar energi ionisasi juga semakin besar semakin negatif afinitas elektron. M g e M. Afinitas Elektron adalah Energi baik yang dibutuhkan maupun yang dilepaskan oleh atomion berfase gas untuk menangkap 1 elektron ket. 261 Energi ionisasi dan afinitas elektron Energi yang diperlukan untuk membuat n1 keadaan valensi ionik dengan mengeluarkan sebuah elektron dari keadaan valensi ionik n dari sebuah bahan disebut sebgai energi ionisasi ke n1.
Unsur golongan IIA dan VIIIA tidak membentuk ion negatif yang stabil.
Dengan demikian proses yang terjadi dapat dipandang sebagai kebalikan dari proses pelepasan elektron yaitu. Semakin besar energi yang dilepas ion negatif yang terbentuk semakin stabil. Cari tahu tentang energi ionisasi dan afinitas elektron yuk. Membutuhkan Energi -.
 Source: slideshare.net
Source: slideshare.net
Membutuhkan Energi -. Dengan demikian proses yang terjadi dapat dipandang sebagai kebalikan dari proses pelepasan elektron yaitu. Membutuhkan Energi -. Karena energi dilepas maka harga afinitas elektron diberi tanda minus. Energi ionisasi berhubungan dengan pembuatan kation dari atom netral dan afinitas elektron berhubungan dengan.
 Source: infostudikimia.blogspot.com
Source: infostudikimia.blogspot.com
O g e O g Electron Affinity. Mereka sangat kecil sehingga kita bahkan tidak bisa mengamati dengan mata telanjang. Sifat Keperiodikan Energi Ionisasi Energi ionisasi adalah energi yang diperlukan suatu atom untuk melepaskan satu elektron valensi membentuk ion positif. Cari tahu tentang energi ionisasi dan afinitas elektron yuk. O g e O g Electron Affinity.
 Source: nawikimia.com
Source: nawikimia.com
- Melepaskan Energi Karena. Harga afinitas elektronnya positifDalam satu periode dari kiri ke kanan nilai afinitas elektron cenderung meningkat. O g e O g Electron Affinity. Secara konvensional definisi energi afinitas adalah energi yang dibebaskan bila tiap mol atom netral atau ion dalam keadaaan gas menangkap elektron membentuk ion negatif. Energi ionisasi dan afinitas elektron berkaitan dengan besarnya daya tarik elektron.
Situs ini adalah komunitas terbuka bagi pengguna untuk berbagi apa yang mereka cari di internet, semua konten atau gambar di situs web ini hanya untuk penggunaan pribadi, sangat dilarang untuk menggunakan artikel ini untuk tujuan komersial, jika Anda adalah penulisnya dan menemukan gambar ini dibagikan tanpa izin Anda, silakan ajukan laporan DMCA kepada Kami.
Jika Anda menemukan situs ini bermanfaat, tolong dukung kami dengan membagikan postingan ini ke akun media sosial seperti Facebook, Instagram dan sebagainya atau bisa juga save halaman blog ini dengan judul energi ionisasi dan afinitas elektron dengan menggunakan Ctrl + D untuk perangkat laptop dengan sistem operasi Windows atau Command + D untuk laptop dengan sistem operasi Apple. Jika Anda menggunakan smartphone, Anda juga dapat menggunakan menu laci dari browser yang Anda gunakan. Baik itu sistem operasi Windows, Mac, iOS, atau Android, Anda tetap dapat menandai situs web ini.





